Recientemente, la Administración Estatal de Alimentos y Medicamentos de China (SFDA) aceptó oficialmente la solicitud de comercialización de tafolecimab (anticuerpo monoclonal PCSK-9 fabricado por INNOVENT BIOLOGICS, INC), INC para el tratamiento de la hipercolesterolemia primaria (incluida la hipercolesterolemia familiar heterocigota y la hipercolesterolemia no familiar). hipercolesterolemia) y dislipidemia mixta.Este es el primer inhibidor de PCSK-9 de producción propia que se solicita para su comercialización en China.
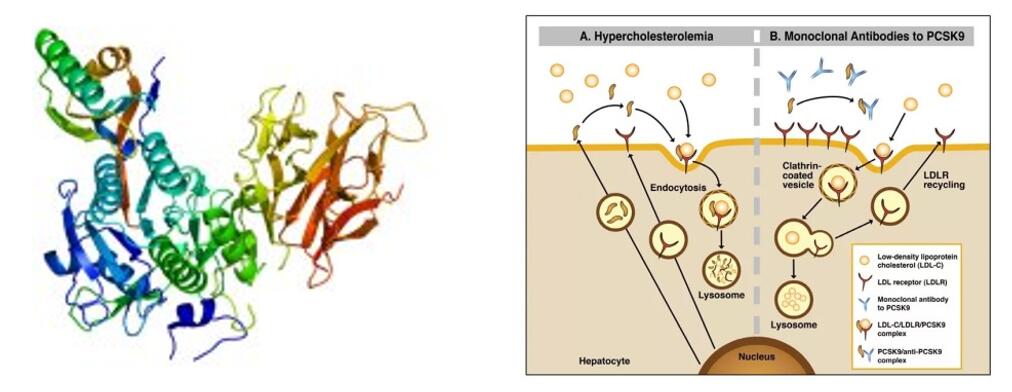
Tafolecimab es un fármaco biológico innovador desarrollado de forma independiente por INNOVENT BIOLOGICS, INC. El anticuerpo monoclonal humano IgG2 se une específicamente a PCSK-9 para aumentar los niveles de LDLR al reducir la endocitosis mediada por PCSK-9, lo que aumenta la eliminación de LDL-C y reduce los niveles de LDL-C.
En los últimos años, la prevalencia de dislipidemia ha aumentado significativamente en China.La prevalencia de dislipidemia e hipercolesterolemia en adultos alcanza el 40,4% y el 26,3% respectivamente.Según el informe de 2020 sobre Salud y Enfermedades Cardiovasculares en China, la tasa de tratamiento y control de la dislipidemia en adultos aún se encuentra en un nivel bajo, y la tasa de cumplimiento de LDL-C de los pacientes con dislipidemia es aún menos satisfactoria.
Anteriormente, las estatinas eran el tratamiento principal para la hipercolesterolemia en China, pero muchos pacientes aún no lograron el objetivo de tratamiento de reducción de LDL-C después del tratamiento.La comercialización de PCSK-9 ha aportado una mayor eficacia a los pacientes.
La presentación de tafolecimab por parte de INNOVENT BIOLOGICS, INC se basa en los resultados de tres ensayos clínicos registrados en una etapa democrática, tiene un buen perfil de seguridad general, similar a las características de seguridad de los productos comercializados, y ha logrado intervalos largos (cada 6 semanas) de administracionLos resultados del estudio CREDIT-2 fueron aceptados por la Reunión Anual de 2022 del Colegio Americano de Cardiología (ACC) como resumen y publicados en línea.
Si se aprueba la solicitud, se romperá el estancamiento de PCSK-9 impoeted, China se convertirá en el cuarto país en tener PCSK-9 después de los Estados Unidos (Amgen), Francia (Sanofi) y Suiza (Novartis).
Hora de publicación: 04-jul-2022