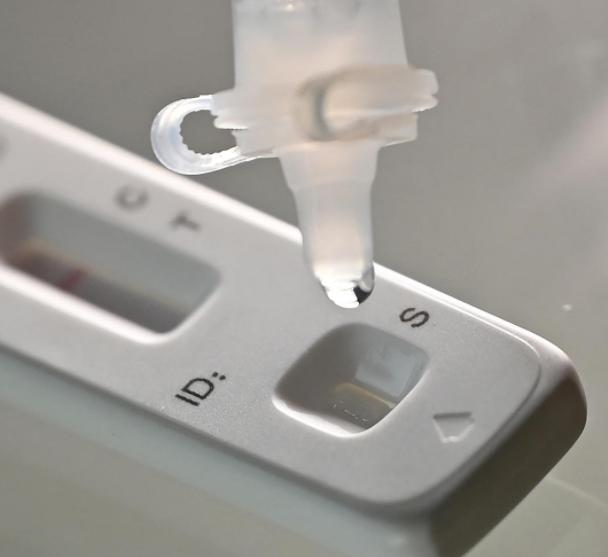
el 12 de marzoth 2022, laNMPA (SFDA) emitió un aviso que aprueba el cambio de solicitud para la autoprueba de productos de antígeno COVID-19 por parte de Nanjing Vazyme BiotechCo., Ltd, Tecnología de bioingeniería de Beijing JinwofuCo., Ltd, Shenzhen Huada Yinyuan Tecnología farmacéutica Co., Ltd., Guangzhou Wondfo Biotech Co., Limitado yBeijing sabio biotecnología co., ltd(huákeTai).Se han lanzado cinco productos de autodiagnóstico de antígenos COVID-19.
El 11 de marzo de 2022, el NHC había anunciado que, con el fin de optimizar aún más la estrategia de prueba de Novel Coronavirus y satisfacer las necesidades de prevención y control de COVID-19, el Equipo Integral del Mecanismo Conjunto de prevención y control del Consejo de Estado decidió agregar pruebas de antígenos a pruebas de ácidos nucleicos y realizó el "Protocolo de aplicación para la detección de antígenos de nuevos coronavirus (ensayo)"
El protocolo especifica la población aplicable para la prueba de antígeno:
Primero, aquellos que visitan instituciones médicas primarias y tienen síntomas como vías respiratorias y fiebre dentro de los 5 días posteriores al inicio de los síntomas;
En segundo lugar, el personal de observación de cuarentena, incluida la observación de cuarentena domiciliaria, el contacto cercano y el subcontacto cercano, la observación de cuarentena de entrada, el personal del área de contención y del área de control;
El tercero son los residentes de la comunidad que tienen la necesidad de autodetección de antígenos.
Consejos: la detección de antígenos es un complemento importante de la detección de ácidos nucleicos, pero los resultados de la autodetección de antígenos no se pueden utilizar como base para el diagnóstico de infección.
Hora de publicación: 22-mar-2022